周谦 高笑男 高敬林 冯章英 王明霞


摘 要 目的:系統评价抗凝药物预防或治疗癌症患者静脉血栓栓塞症(VTE)的药物经济性。方法:计算机检索PubMed、Embase、Cochrane图书馆、中国知网、万方数据、维普网、中国生物医学文献服务系统以及The NHS Economic Evaluation Database、The Healthy Technology Assessment Database、EconLit等数据库,并辅以手工检索,收集不同抗凝药预防或治疗癌症患者VTE的经济学评价研究,检索时限为建库至2020年11月12日。经筛选、提取后,采用卫生经济评估报告标准清单评价纳入文献的质量。采用描述性的方法总结纳入文献的基本特征,并根据用药目的和不同干预分组归纳其经济学结果。结果:共纳入15篇文献,3篇质量优秀,10篇质量良好,其余2篇质量适中。研究分布于中国(1项)、美国(7项)、加拿大(3项)、法国(2项)、荷兰(1项)、巴西(1项)、奥地利(1项)等不同收入水平的国家。对于预防癌症患者VTE,华法林和低分子肝素(LMWH)的经济学评价有待更新;在VTE中高风险的癌症患者中,新型口服抗凝药(NOACs)在中国的经济优势不如美国,但是其在VTE高风险人群中的经济优势却在增加;阿司匹林对比依诺肝素预防骨髓瘤患者VTE具有绝对经济优势。对于治疗癌症患者VTE,LMWH对比华法林在美国不具有成本-效用优势,但是在加拿大和北欧等国家具有明显的经济优势;NOACs对比LMWH能节省总成本,但是美国和巴西的增量效果正负相反。敏感性分析显示,经济学结果对药物价格、血栓发生风险基线率以及不同干预下的不良事件(血栓复发、大出血、死亡)发生风险敏感,其中药物价格和血栓发生基线率能够逆转结论。结论:对于预防癌症患者VTE,与无干预或安慰剂相比,NOACs在不同国家、不同血栓风险人群中的经济性不同;华法林、LMWH的经济性尚未明确;阿司匹林对比依诺肝素的经济优势明显。对于治疗癌症患者VTE,LMWH对比华法林在不同国家的经济优势不同;NOACs对比LMWH能节省成本。经济策略受不同国家的疾病发生风险、医疗体系、药物价格、患者偏好和价值观以及经济水平、成本-效用阈值标准等影响较大,最终的经济决策需要依据不同国家背景而定。
关键词 抗凝药物;癌症;静脉血栓栓塞症;药物经济学;系统评价
中图分类号 R956 文献标志码 A 文章编号 1001-0408(2021)07-0850-10
ABSTRACT OBJECTIVE:
To systematically review the pharmacoeconomics of anticoagulants for the prevention and therapy of venous thromboembolism (VTE) in cancer patients. METHODS:
Retrieved from PubMed, Embase, Cochrane library, CNKI, Wanfang database, VIP, SinoMed, The NHS Economic Evaluation Database, The Healthy Technology Assessment Database and EconLit, supplemented by manual retrieval, the economic evaluation studies on the prevention and therapy of VTE in cancer patients with different anticoagulants were collected. The retrieval time was from the inception to Nov. 12th, 2020. After screening and extracting, the Consolidated Health Economic Evaluation Reporting Standards (CHEERS) was used to evaluate the quality of the included literatures. The basic characteristics of the included literatures were summarized by descriptive methods, and the economic results were summarized according to medication purpose and different intervention grouping. RESULTS:
A total of 15 literatures were included. Three literatures were of excellent quality; ten were of good quality; and the other two were of moderate quality. Included studies were widely conducted in countries of different economic levels, including China (1 piece), the United States (7 pieces), Canada (3 pieces), France (2 pieces), the Netherlands (1 piece), Brazil (1 piece) and Austria (1 piece). For preventing VTE in cancer patients, the economic evaluation results of warfarin and low-molecular-weight heparin (LMWH) needed to be updated. Novel oral anticoagulants (NOACs) for the prevention of VTE were less cost-effective among cancer patients with medium- and high-risk venous thrombosis in China than in the United States, but the economic advantage increased among the high-risk patients. Compared to enoxaparin, aspirin was absolutely dominant to preventing VTE in patients with myeloma. For the treatment of VTE in cancer patients, LMWH was not cost-effective, compared to warfarin in the United States; but it was cost-effective in Canada and some countries of Northern Europe. Compared with LMWH, NOACs could save total cost, but the incremental utility in the United States and Brazil were opposite. Sensitivity analysis showed that economic results were sensitive to drug prices, the baseline rate of thrombosis risk, and the risk of adverse events (thrombosis recurrence, major bleeding and death) of different interventions, the first two of which could reverse the conclusions. CONCLUSIONS:
For the prevention of VTE in cancer patients, compared with no intervention or placebo, the economic advantages of NOACs were different in different countries or for patients with different thrombosis risk; the economics of warfarin and LMWH were not yet clear. Aspirin had obvious economic advantages compared with enoxaparin. For the treatment of VTE in cancer patients, LMWH had different economic advantages compared with warfarin in different countries; NOACs could save costs compared with LMWH. Economic strategies are greatly affected by the risk of diseases, medical systems, drug price, patient preferences and values, economic levels, cost-utility threshold standards in different countries. Therefore, the final economic strategies need to be based on the contexts of different countries.
KEYWORDS Anticoagulants; Cancer; Venous thromboembolism; Pharmocoeconomics; Systematic review
静脉血栓栓塞症(VTE)是造成癌症患者死亡的重要原因之一,主要包括深静脉血栓(DVT)和肺栓塞(PE)[1]。在癌症患者中,VTE的累计发生率约为1%~8% ,是普通患者血栓风险的4.1倍[2]。同时,癌症相关血栓(CAT)患者在抗凝治疗期间还面临复发和出血的风险[1]。最近一项研究发现,伴有VTE的癌症患者住院率是不伴有VTE的癌症患者的3倍,且医疗费用增加了30 538美元[3]。因此,预防或治疗癌症患者VTE不仅需要考虑抗凝药物的安全性和有效性,而且还需要关注其经济性。
目前,用于防治VTE的抗凝药物包括普通肝素(UFH)、低分子肝素(LMWH)、磺达肝癸钠(Fondaparinux)、华法林(Warfarin)、新型口服抗凝剂(NOACs)等。最新国内外指南均建议在血栓高风险(Khorana评分≥3)的门诊化疗癌症患者以及多发性骨髓瘤患者中进行VTE预防[2,4]。美国临床肿瘤协会(ASCO)和国际血栓与止血学会(ISTH)相关指南建议采用利伐沙班(Rivaroxaban)作为癌症患者VTE的一级预防用药,该药适用的癌症患者范围更广泛,包括起始化疗、血栓中高风险(Khorana评分≥2)、无药物相互作用且无出血高风险(如胃肠道癌症)的门诊癌症患者[1,5]。依据血栓发生部位和复发风险,指南建议伴有VTE的癌症患者的抗凝时间至少持续3~12个月,甚至无限期抗凝[2,4]。目前,针对癌症患者防治VTE的抗凝药物的有效性和安全性研究较多,但缺乏此类药物经济性的相关研究[5-6]。因此,本文通过系统检索、总结归纳防治癌症患者VTE的抗凝药物的经济学研究,为临床合理用药和医药卫生决策提供经济学依据。
1 资料与方法
1.1 纳入与排除标准
1.1.1 纳入标准
(1)研究类型:防治癌症患者VTE的抗凝药物的经济学分析,包括成本-效果分析、成本-效用分析、成本-效益分析和最小成本分析等;(2)语种:限定为中、英文。
1.1.2 研究对象
(1)癌症患者,伴有或不伴有VTE;(2)非癌症外科围手术期抗凝的患者。
1.1.3 干预措施
美国国家综合癌症网络临床实践指南《癌症相关性静脉血栓栓塞性疾病(2020.V1)》[4]和中国《肿瘤相关静脉血栓栓塞症预防与治疗指南(2019版)》[2]推荐的预防或治疗VTE用药,包括UFH、LMWH、磺达肝癸钠、华法林、利伐沙班、艾多沙班(Edoxaban)、阿哌沙班(Apixaban)等;对于预防用药,其对照干预措施除了上述药物外,还可以为无干预或安慰剂或预防骨髓瘤患者VTE的阿司匹林(Aspirin)。
1.1.4 结局指标
成本、质量调整生命年(QALYs)、增量成本-效果比(ICER)、增量成本-效用比(ICER)等经济学评价指标。
1.1.5 排除标准
(1)研究对象不符合的文献;(2)干预措施不包括抗凝药物的文献;(3)经济学评价指标不明确的文献;(4)综述、摘要以及其他无法获取全文的文献。
1.2 文献检索策略
计算机检索中外医学、卫生技术评估、经济学数据庫,如PubMed、Embase、Cochrane图书馆、中国知网、万方数据、维普网、中国生物医学文献服务系统(SinoMed)以及The NHS Economic Evaluation Database(NHS EED)、The Healthy Technology Assessment Database(HTA)、EconLit等,并对检索到的相关综述文献辅以手工检索;检索时限为各数据库建库至2020年11月12日。采用主题词、关键词和自由词相结合的检索方式,依具体数据库调整。英文检索主题词为“Cost-benefit analysis”“Anticoagulants”“Thromboembolism”“Neoplasms”,关键词及自由词为“Cost benefit”“Cost utility”“Cost effectiveness”“Cost analysis”“Economic”“Pharmacoeconomic”“Marginal”“Heparin”“Dicumarol”“Coumarins”“NOACs”“DOACs”“UFH”“LMWH”“Enoxaparin”“Dalteparin”“Tinzaparin”“Warfarin”“Vitamin K antagonist”“Fondaparinux”“Rivaroxaban”“Edoxaban”“Apixaban”“Dabigatran”“Aspirin”“Venous”“Thrombosis”“Embolism”“VTE”“DVT”“PE”“Tumor”“Cancer”;中文检索词为与之对应词。以Cochrane图书馆为例,检索策略如图1所示。
1.3 数据提取
按照上述纳入与排除标准,由2名研究者独立收集文献和提取数据;若存在分歧,则由第3名研究者进行评审。总结、提取纳入文献的第一作者、时间、研究对象、干预措施、评价方法和经济学评价结果等信息。
1.4 文献质量评价
采用卫生经济评估报告标准清单(CHEERS)评估文献报告质量[7]。该清单包括“题目与摘要”“介绍”“方法”“结果”“讨论”“其他”等6个部分——若文献完全符合标准,记1分;若不满足或不充分,记0分;其他,记“不适用”。对于“讨论”部分,若文献同时满足“结果”和“局限性”2项,且至少满足“适用性”或“当前知识”中的1项,记1分。评价结果以总得分占最大可能得分的百分比表示,分为优秀(100%符合)、良好(75%~99%符合)、适中(50%~74%符合)和偏低(不足50%符合)等4个等级[7]。由2名研究者打分,存在分歧时请第3名研究者判断后打分。为确保研究文献的质量可靠性,剔除质量等级为“偏低”的文献。
1.5 数据处理
采用描述性的方法总结文献的基本特征,按照用药目的和不同干预分组归纳所纳入文献的经济学结果。
2 结果
2.1 文献检索结果
从各数据库中共检索出文献703篇,去重后剩余550篇;经标题和摘要初筛后获得44篇;阅读全文后最终纳入15篇。文献检索流程与结果如图2所示。
2.2 纳入文献的基本特征
共纳入15篇文献[8-22],发表于1995-2020年;美国7篇[9-10,12,15,18-19,21],加拿大3篇[8,11,16],法国2篇[13,17],中国[20]、荷兰[14]、巴西[22]、奥地利[17]各1篇。其中,5篇研究分析了預防癌症患者VTE的药物的经济性[8,12-13,20-21],1篇研究分析了癌症患者住院治疗VTE的短期经济性[9],其余9篇研究分析了治疗癌症患者VTE并进行扩展预防的药物的经济性[10-11,14-19,22]。进行比较的药物包括UFH、华法林、LMWH、NOACs和阿司匹林,其中LMWH包括依诺肝素(Enoxaparin)和达肝素(Dalteparin),NOACs包括利伐沙班、阿哌沙班和艾多沙班。最早发表的2篇研究的评价方法采用的是最小成本分析[8-9],其余13篇文献均进行了成本-效用分析[10-22]。研究时限为4个月至终生。纳入文献的基本特征如表1所示。
2.3 纳入文献的质量评价
所有文献均符合CHEERS清单报告要求[7]。其中,3篇评分为100%[11,14,16],质量优秀;10篇评分为75%~99%[8-10,12-13,17,19-22],质量良好;其余2篇评分分别为72%和63%[15,18],质量适中。所有纳入文献的“前言”和“讨论”部分得分均为100%,“方法”部分存在的问题主要是未阐述模型、研究角度和研究时限的选择理由,对比较对象的用法用量、参数分析方法以及效果来源的描述不充分。4篇文献未体现贴现率[9,12,16,18],其中3篇研究时限不足1年[9,16,18]。“结果”部分存在的问题主要是不确定性分析不够全面。只有最早发表的2篇文献未完全体现“资金来源”和“利益冲突”条目[8-9]。
2.4 纳入文献的主要临床效果
纳入文献的主要临床效果来源如表1所示。
Avritscher等[9]通过收集病历建立回顾性队列以获得临床效果。该研究通过匹配试验组和对照组患者的年龄、肿瘤表现、分期以及VTE病史等因素来降低组间异质性,但由于达肝素组样本量过小,故假设达肝素的临床效果与UFH一致。其余研究的临床效果主要源于临床RCT和Meta分析[8,10-22]。当研究时限超出RCT的随访时间后,Li等[19,21]的研究在模型中使用了大型流行病学研究方法以及美国生命表数据来模拟随时间变化的转移概率[31,36-37]。
文献研究结果显示,对于预防癌症患者VTE,与安慰剂或无干预预防比较,使用4、6个月的VLDW、LMWH以及低剂量NOACs均能有效降低VTE发生率,但不会明显降低患者病死率,其中低剂量NOACs的出血风险更高[23,25,34-35]。AVERT研究表明,相比于安慰剂,阿哌沙班能够明显提高患者的大出血率[3.5% vs. 1.8%;HR=2.00,95%CI(1.01,3.95),P=0.046],其中胃肠道或妇科癌症患者的出血风险更高[32]。基于CASSINI、AVERT研究的Meta分析和累积分析结果均表明,在具有VTE中高风险(Khorana评分≥2)的化疗癌症患者中,低剂量NOACs(如阿哌沙班、利伐沙班)较安慰剂有增加出血风险的趋势,但差异无统计学意义[32-35]。Li等[35]的Meta分析显示,低剂量NOACs在VTE高风险癌症患者中的疗效优于VTE低风险组。在骨髓瘤患者中,阿司匹林与依诺肝素预防癌症患者VTE的疗效和安全性无明显差异[26]。
对于治疗癌症患者VTE,CLOT研究以及Meta分析结果均显示,与华法林相比,LMWH可明显降低VTE复发率,同时不提高出血率,其中中重度肾损伤患者疗效受益更加明显(3% vs. 17%;P=0.011)[15,24,27]。基于Hokusai VTE cancer和SELECT-D研究的Meta分析显示,NOACs降低VTE复发的疗效优于达肝素,但前者可增加大出血的风险[28-29],其中胃肠道癌症患者的出血风险更高[30]。Raskob等[38]的研究结果显示,艾多沙班降低VTE复发率的疗效不劣于华法林,同时未提高出血率。上述研究均未能证实不同干预下癌症患者的病死率存在明显差异。
2.5 纳入文献的经济学评价结果
2.5.1 癌症患者VTE预防用药
Rajan等[8]的研究表明,在初始化疗的转移性乳腺癌患者中,与使用安慰剂相比,每100名患者连续使用6个月VLDW的药物成本增加了21 854加元,但不良反应成本减少了24 297加元,最终总成本减少了2 433加元。
Pishko等[12]的研究表明,在门诊癌症患者中,当死亡相对风险为0.920时,若选取较高的成本-效用阈值(以下简称“阈值”)即100 000美元,与无干预相比,使用依诺肝素4个月更具有成本-效用优势;但是不建议将干预时间延长至24个月,除非死亡相对风险低于0.762。
Du等[20]和Li等[21]分别基于中国和美国背景研究了在具有VTE中高风险(Khorana评分≥2)的化疗癌症患者中预防性使用低剂量NOACs 6个月的长期经济性。这2项研究均表明,与安慰剂相比,低剂量NOACs的QALYs更高。在中国,当以人均国内生产总值(GDP)的1倍作为阈值时,NOACs不具有成本-效用优势;而在美国,NOACs与安慰剂相比的ICER远低于阈值,具有明显的成本-效用优势;此外,无论中国还是美国,NOACs在VTE高风险(Khorana评分≥3)亚组患者中的成本-效用优势均明显增加。鉴于目前NOACs在中国价格偏高,Du等[20]的研究并不强烈推荐使用NOACs来预防VTE,最终应根据癌症患者的病死率、血栓和出血风险调整预防策略。
Chalayer等[13]的研究表明,在接受沙利度胺治疗的新确诊多发性骨髓瘤患者中,与依诺肝素相比,使用阿司匹林预防VTE 6个月不仅能降低成本,而且能够提高患者的生存质量,具有绝对经济优势。
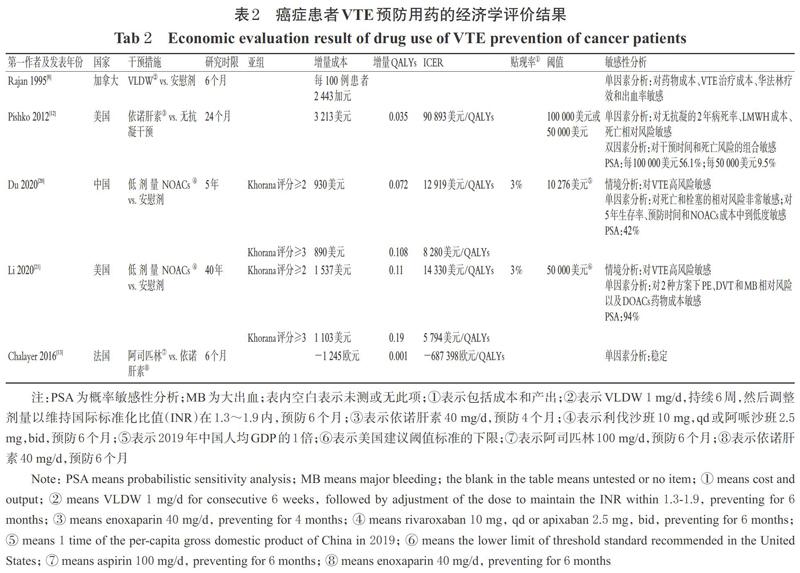
癌症患者VTE预防用药的经济学评价结果如表2所示。
2.5.2 癌症患者VTE治疗用药
(1)LMWH对比华法林:美国的2项研究均表明,在伴有VTE的癌症患者中,LMWH的QALYs较华法林更高;但LMWH的药物成本过高,使其与华法林相比的ICER远超过其阈值,因此华法林更加经济[10,15]。
然而,Dranitsaris等[11,14,16-17]的系列研究显示,在加拿大以及荷兰、法国和奥地利等北欧国家,相比华法林,LMWH治疗癌症患者VTE 6个月的成本-效用优势更加明显。在中重度肾损伤癌症患者中,LMWH具有潜在的绝对经济优势[14,16-17]。Dranitsaris等[11]对前瞻性临床试验CLOT研究的患者个体数据进行了多因素分析,发现达肝素干预、男性、年龄和癌症表现状态等因素能够明显影响药物治疗成本,其中达肝素干预、男性均可导致患者治疗成本增加;且患者年龄越大、肿瘤表现状态评分越差,其病死率更高,可能导致总成本降低。
从上述2种策略的成本组成来看,达肝素干预的药物成本占比最多,远远超过华法林(46%~67% vs. 3%~13%)[11,14-15],而华法林的VTE治疗成本和实验室监测成本占比最多[11]。
LMWH对比华法林治疗癌症患者VTE的经济学评价结果如表3所示。
(2)NOACs对比LMWH、华法林以及其他药物:在美国和巴西,NOACs较达肝素治疗癌症患者VTE更能节省成本[18-19,22]。不同的是,在美国,NOACs的QALYs略低于达肝素,但由于其成本远低于LMWH而具有经济性[18-19];而在巴西,NOACs的QALYs高于达肝素,因此NOACs是绝对经济策略[22]。无论是否针对胃肠道癌症患者,NOACs均因成本远远低于LMWH而更经济[18-19]。胃肠道癌症患者使用NOACs的总成本因出血风险的增加而增加,但不足以使LMWH对比NOACs的ICER低于阈值[18]。
Lopes等[22]的研究表明,当以巴西人均GDP的3倍作为阈值时,与华法林比较,艾多沙班治疗癌症患者VTE具有明显成本-效用优势。
Avritscher等[9]的研究表明,在因VTE的住院治疗中,与UFH比较,达肝素能够通过缩短癌症患者住院时间和减少其监测次数而具有最小成本。
NOACs对比LMWH、华法林以及其他药物治疗癌症患者VTE的经济学评价结果如表4所示。
2.6 敏感性分析结果
纳入文献均进行了敏感性分析,结果如表2~表4所示。其中,14篇文献进行了单因素分析[8-17,19-22],2篇进行了双因素分析[12,18],3篇进行了情境分析[19,20-21],6篇进行了PSA[10,12,19-22]。
2.6.1 癌症患者VTE预防用药
对于预防癌症患者VTE,药物成本是经济策略的共同驱动因素[8,12,20-21]。Rajan等[8]的研究显示,增量成本对VTE治疗成本、华法林疗效、大出血等不良事件发生相对风险敏感,即当不良事件发生率提高、VTE的治疗成本降低时,VLDW的经济优势会进一步降低。Pishko等[12]的研究表明,依诺肝素对比安慰剂的死亡相对风险是驱动经济结果的关键因素,而依诺肝素效果对其ICER的影响并不明显。
无论在中国还是美国,低剂量NOACs对比安慰剂的ICER对发生VTE、MB和死亡事件的相对风险等因素高度敏感,而对药物成本、预防时间和患者5年生存率变化等因素的敏感程度较小[20-21]。在中国,癌症人群的VTE风险基线率会逆转NOACs对比安慰剂的经济学结论[20]。PSA结果显示,NOACs在美国具有成本-效用优势的概率明显高于中国(94% vs. 42%~55%)[20-21]。除VTE风险基线率外,其他参数的变化不会改变低剂量NOACs对比安慰剂的经济决策[20-21]。
2.6.2 癌症患者VTE治疗用药
药物成本始终是美国治疗癌症患者VTE经济策略的主要驱动因素[10,15,18-19],而对其他国家的影响不明显。在美国,相比华法林或者NOACs,当达肝素价格降低或者替换为更便宜的依诺肝素时,LMWH可能逆转原先不经济的结论[10,18-19]。LMWH对比华法林、NOACs的ICER对干预下的死亡相对风险敏感[10,19],当死亡相对风险降低时,经济策略有利于LMWH。在NOACs对比LMWH的经济学评价中,研究时限(12、60个月)对增量成本影响较大,干预下的死亡相对风险和相对效用值对增量效果影响较明显[19]。然而,PSA结果显示,尽管ICER随上述参数(除成本外)变化,但是不会改变最终的经济决策[10,18-19]。
3 讨论
VTE是癌症的严重并发症之一,增加了患者的额外负担[3]。因此,本研究对抗凝药物防治癌症患者VTE的经济学研究进行了系统评价,并从经济学角度探讨了不同抗凝药物预防和治疗癌症患者VTE的优劣以及影响其经济性的因素。
本研究发现,对于初始化疗或具有VTE中高风险(Khorana评分≥2)的癌症患者,预防性抗凝均能改善患者的生存质量,并且在合理的预防时间内具有成本-效用优势[8,12-13,20-21]。Li等[21]通过经济学研究发现,低劑量NOACs在抗凝结束(6个月)与之后5年的临床结局相似,提示早期预防对癌症患者具有长期积极作用。当患者血栓风险趋于平稳后,若延长预防时间,成本和效果可能同时增加,但边际效应降低,最终导致方案不再具有经济性[12,21]。
相比无干预或安慰剂,华法林和LMWH的流行病学更新数据显示,两者预防癌症患者VTE的出血风险明显增加,而患者病死率没有明显降低[39-40]。这将降低预防策略的经济优势,也提示需要根据最新证据和当前经济水平重新评估华法林和LMWH预防VTE的经济性。低剂量NOACs对比安慰剂预防癌症患者VTE的临床效果源自AVERT研究和CASSINI研究,其对患者的VTE风险分层均是基于Khorana风险评估模型[32-33]。该模型存在一定的不足之处,例如在肺癌中表现不佳、未考虑化疗方案等[34],因此风险评估模型的局限性可能会影响评价结果的适用性。
对于治疗癌症患者VTE,LMWH对比华法林在不同国家的价格差异十分明显,因而经济策略不同[10-11,14-19,22]。NOACs对比LMWH的价格优势可减少VTE复发的疗效,抵消NOACs导致的出血成本[28,30]。因此,NOACs对比LMWH能够明显节省成本。需要注意的是,NOACs在胃肠道癌症患者中的出血风险较高,因此国内外指南均不推荐将NOACs应用于此类患者[2,4]。存在争议的是,NOACs对比LMWH的增量QALYs在美国为负值,而在巴西为正值,这可能与不同国家患者用药偏好和疗效偏好的差异有关:首先,NOACs可直接口服,能减少注射带来的痛苦;再者,Hokusai-VTE Cancer研究和相关Meta分析结果均显示,NOACs对比LMWH虽然会增加出血风险,但是也会降低VTE复发率,出血风险和疗效对QALYs的影响恰好相反[28,30]。德国和英国的2项研究显示,无论是癌症患者还是护理者均会优先权衡抗凝药物的疗效和出血风险,并且在血栓和出血风险相似的前提下,才倾向于选择口服用药的方式[41-42]。然而,这可能与中低收入国家(例如巴西)的患者选择偏好存在差异。目前,尚缺乏相关研究直接评估癌症患者对NOACs和LMWH的选择偏好。
藥物成本是防治癌症患者VTE经济策略的主要驱动因素[8,10,12,15,18-21]。对于预防癌症患者VTE,降低药物成本必然增加预防策略的经济性,尤其是对于VTE高风险(Khorana评分≥3)的癌症患者。其中,LMWH的经济学评价结果对价格高度敏感[10,12,15,18-19]。目前,国内临床广泛应用的LMWH选择多、价格各异,并且不同的LMWH的临床效果也可能存在差异[43-44]。因此,基于真实世界的医疗数据对不同LMWH之间以及LMWH与口服抗凝药进行经济学评价具有实际价值。其他影响评价结果的因素主要是不同干预下发生或复发VTE、大出血和死亡的相对风险。当试验组对比对照组的不良事件发生率降低时,增量效果增加[8,10,12,19-21]。目前,尚无临床证据确切表明任何抗凝策略能够明显降低癌症患者的病死率[6,27,30,39-40,45]。
本研究尚存在一定局限性:一是只检索已发表的文献,未纳入灰色文献;二是纳入文献质量不齐;三是经济学结果无法定量分析。由于研究人群、方法等不一致,并且没有华法林、LMWH和NOACs之间的直接比较,所以本研究未能得出何种抗凝药物预防癌症患者VTE最经济。此外,本研究纳入的NOACs 对比华法林的直接比较研究较少。目前,华法林由于价格低廉,可能在低收入地区更常用。随着NOACs的广泛应用及其在价格和疗效上的优势逐渐凸显,该药相比华法林在低收入地区可能将更具有经济优势。因此,需要进一步研究证实NOACs对比华法林治疗癌症患者VTE的经济性。
综上,防治癌症患者VTE的药物经济学评价结果受不同国家的医疗体系、药物价格、患者偏好和价值观以及经济水平、阈值标准等影响明显,缺乏一致性和可比性;而且,各国的疾病发生风险、治疗指南、临床路径以及医师用药习惯等亦存在差异。因此,国外研究结果并不完全适用于国内,亟需开展更多中国人群防治癌症患者VTE的药物经济学研究,为我国临床决策和药品政策制定提供可靠证据。
参考文献
[ 1 ] KEY N S,KHORANA A A,KUDERER N M,et al. Venous thromboembolism prophylaxis and treatment in patients with cancer:ASCO clinical practice guideline update[J]. J Clin Oncol,2020,38(5):496-520.
[ 2 ] 马军,秦叔逵,吴一龙,等.肿瘤相关静脉血栓栓塞症预防与治疗指南:2019版[J].中国肿瘤临床,2019,46(13):653-660.
[ 3 ] STREIFF M,MILENTIJEVIC D,MCCRAE K R,et al. Healthcare resource utilization and costs associated with venous thromboembolism in cancer patients treated with anticoagulants[J]. J Med Econ,2019,22(11):1134-1140.
[ 4 ] NCCN. NCCN clinical practice guidelines in oncology:cancer-associated venous thromboembolic disease:2020.V1[EB/OL]. [2020-04-16]. https://www.nccn.org/disclosures/guidelinepanellisting.aspx.
[ 5 ] WANG T F,ZWICKER J I,AY C,et al. The use of direct oral anticoagulants for primary thromboprophylaxis in ambulatory cancer patients:guidance from the SSC of the ISTH[J]. J Thromb Haemost,2019,17(10):1772-1778.
[ 6 ] 張嘉俊,杨琰茗,杨雅清,等. Ⅹa因子抑制剂预防和治疗癌症患者静脉血栓栓塞有效性和安全性的Meta分析[J].中国药房,2020,31(6):729-733.
[ 7 ] HUSEREAU D,DRUMMOND M,PETROU S,et al. Con- solidated health economic evaluation reporting standards (CHEERS):explanation and elaboration:a report of the ISPOR health economic evaluation publication guidelines good reporting practices task force[J]. Value Health,2013,16(2):231-250.
[ 8 ] RAJAN R,GAFNI A,LEVINE M,et al. Very low-dose warfarin prophylaxis to prevent thromboembolism in women with metastatic breast cancer receiving chemothe- rapy:an economic evaluation[J]. J Clin Oncol,1995,13(1):42-46.
[ 9 ] AVRITSCHER E B,CANTOR S B,SHIH Y C,et al. Cost- minimization analysis of low-molecular-weight heparin (dalteparin) compared to unfractionated heparin for inpatient treatment of cancer patients with deep venous thrombosis[J]. Support Care Cancer,2004,12(7):531-536.
[10] AUJESKY D,SMITH K J,CORNUZ J,et al. Cost-effectiveness of low-molecular-weight heparin for secondary prophylaxis of cancer-related venous thromboembolism[J]. Thromb Haemost,2005,93(3):592-599.
[11] DRANITSARIS G,VINCENT M,CROWTHER M. Dal- teparin versus warfarin for the prevention of recurrent venous thromboembolic events in cancer patients:a pharmacoeconomic analysis[J]. Pharmacoeconomics,2006,24(6):593-607.
[12] PISHKO A M,SMITH K J,RAGNI M V. Anticoagulation in ambulatory cancer patients with no indication for prophylactic or therapeutic anticoagulation:a cost-effectiveness analysis from a U.S. perspective[J]. Thromb Haemost,2012,108(2):303-310.
[13] CHALAYER E,BOURMAUD A,TINQUAUT F,et al. Cost-effectiveness analysis of low-molecular-weight heparin versus aspirin thromboprophylaxis in patients newly diagnosed with multiple myeloma[J]. Thromb Res,2016,145:119-125.
[14] DRANITSARIS G,SHANE L,BURGERS L,et al. Economic analysis comparing dalteparin to vitamin K antagonists to prevent recurrent venous thromboembolism in patients with cancer having renal impairment[J]. Clin Appl Thromb Hemost,2016,22(7):617-626.
[15] CONNELL N T,ABEL G A,CONNORS J M. Low-molecular weight heparin versus vitamin K antagonists for the treatment of cancer-associated thrombosis:a cost- effectiveness analysis[J]. Thromb Res,2017,150:53-58.
[16] DRANITSARIS G,SHANE L G,CROWTHER M,et al. Dalteparin versus vitamin K antagonists for the prevention of recurrent venous thromboembolism in patients with cancer and renal impairment:a Canadian pharmaco- economic analysis[J]. Clinicoecon Outcomes Res,2017,9:65-73.
[17] DRANITSARIS G,SHANE L G,GALANAUD J P,et al. Dalteparin or vitamin K antagonists to prevent recurrent venous thromboembolism in cancer patients:a patient- level economic analysis for France and Austria[J]. Support Care Cancer,2017,25(7):2093-2102.
[18] CONNELL N T,CONNORS J M. Cost-effectiveness of edoxaban versus dalteparin for the treatment of cancer- associated thrombosis[J]. J Thromb Thrombolysis,2019,48(3):382-386.
[19] LI A,MANOHAR P M,GARCIA D A,et al. Cost effectiveness analysis of direct oral anticoagulant (DOAC) versus dalteparin for the treatment of cancer associated thrombosis (CAT) in the United States[J]. Thromb Res,2019,180:37-42.
[20] DU J,WU B. New oral anticoagulants for thromboprophylaxis in patients with cancer receiving chemotherapy:an economic evaluation in a Chinese setting[J]. Clin Drug Investig,2020,40(7):653-663.
[21] LI A,CARLSON J J,KUDERER N M,et al. Cost-effectiveness analysis of low-dose direct oral anticoagulant (DOAC) for the prevention of cancer-associated thrombosis in the United States[J]. Cancer,2020,126(8):1736- 1748.
[22] LOPES D G,TAMAYO A,SCHIPP B,et al. Cost-effectiveness of edoxaban vs low-molecular-weight heparin and warfarin for cancer-associated thrombosis in Brazil[J]. Thromb Res,2020,196:4-10.
[23] LEVINE M,HIRSH J,GENT M,et al. Double-blind randomised trial of a very-low-dose warfarin for prevention of thromboembolism in stage Ⅳ breast cancer[J]. Lancet,1994,343(8902):886-889.
[24] LEE A Y,LEVINE M N,BAKER R I,et al. Low-molecular-weight heparin versus a coumarin for the prevention of recurrent venous thromboembolism in patients with cancer[J]. N Engl J Med,2003,349(2):146-153.
[25] AKL E A,GUNUKULA S,BARBA M,et al. Parenteral anticoagulation in patients with cancer who have no therapeutic or prophylactic indication for anticoagulation[J]. Cochrane Database Syst Rev,2011(4):CD006652.
[26] PALUMBO A,CAVO M,BRINGHEN S,et al. Aspirin,warfarin,or enoxaparin thromboprophylaxis in patients with multiple myeloma treated with thalidomide:a phase Ⅲ,open-label,randomized trial[J]. J Clin Oncol,2011,29(8):986-993.
[27] AKL E A,KAHALE L,BARBA M,et al. Anticoagulation for the long-term treatment of venous thromboembolism in patients with cancer[J]. Cochrane Database Syst Rev,2014(7):CD006650.
[28] RASKOB G E,VAN ES N,VERHAMME P,et al. Edoxaban for the treatment of cancer-associated venous thromboembolism[J]. N Engl J Med,2018,378(7):615-624.
[29] YOUNG A M,MARSHALL A,THIRLWALL J,et al. Comparison of an oral factor Ⅹ a inhibitor with low molecular weight heparin in patients with cancer with venous thromboembolism:results of a randomized trial (SELECT-D)[J]. J Clin Oncol,2018,36(20):2017-2023.
[30] LI A,GARCIA D A,LYMAN G H,et al. Direct oral anticoagulant (DOAC) versus low-molecular-weight heparin (LMWH) for treatment of cancer associated thrombosis (CAT):a systematic review and meta-analysis[J]. Thromb Res,2019,173:158-163.
[31] CHEE C E,ASHRANI A A,MARKS R S,et al. Predictors of venous thromboembolism recurrence and bleeding among active cancer patients:a population-based cohort study[J]. Blood,2014,123(25):3972-3978.
[32] CARRIER M,ABOU-NASSAR K,MALLICK R,et al. Apixaban to prevent venous thromboembolism in patients with cancer[J]. N Engl J Med,2019,380(8):711-719.
[33] KHORANA A A,SOFF G A,KAKKAR A K,et al. Riva- roxaban for thromboprophylaxis in high-risk ambulatory patients with cancer[J]. N Engl J Med,2019,380(8):720-728.
[34] AGNELLI G. Direct oral anticoagulants for thromboprophylaxis in ambulatory patients with cancer[J]. N Engl J Med,2019,380(8):781-783.
[35] LI A,KUDERER N M,GARCIA D A,et al. Direct oral anticoagulant for the prevention of thrombosis in ambulatory patients with cancer:a systematic review and meta- analysis[J]. J Thromb Haemost,2019,17(12):2141-2151.
[36] COHEN A T,KATHOLING A,RIETBROCK S,et al. Epidemiology of first and recurrent venous thromboembolism in patients with active cancer:a population-based cohort study[J]. Thromb Haemost,2017,117(1):57-65.
[37] MARTINEZ C,COHEN A T,BAMBER L,et al. Epide- miology of first and recurrent venous thromboembolism:a population-based cohort study in patients without active cancer[J]. Thromb Haemost,2014,112(2):255-263.
[38] RASKOB G E,VAN E S N,SEGERS A,et al. Edoxaban for venous thromboembolism in patients with cancer:results from a non-inferiority subgroup analysis of the Hokusai-VTE randomised,double-blind,double-dummy trial[J]. Lancet Haematol,2016,3(8):e379-e387.
[39] AKL E A,KAHALE L A,HAKOUM M B,et al. Paren- teral anticoagulation in ambulatory patients with cancer[J]. Cochrane Database Syst Rev,2017,9(9):CD006652.
[40] KAHALE L A,HAKOUM M B,TSOLAKIAN I G,et al. Oral anticoagulation in people with cancer who have no therapeutic or prophylactic indication for anticoagulation[J]. Cochrane Database Syst Rev,2017,12(12):CD006466.
[41] NOBLE S,MATZDORFF A,MARAVEYAS A,et al. Assessing patients anticoagulation preferences for the treatment of cancer-associated thrombosis using conjoint methodology[J]. Haematologica,2015,100(11):1486- 1492.
[42] HUTCHINSON A,REES S,YOUNG A,et al. Oral anti- coagulation is preferable to injected,but only if it is safe and effective:an interview study of patient and carer experience of oral and injected anticoagulant therapy for cancer-associated thrombosis in the SELECT-D trial[J]. Palliative Med,2019,33(5):510-517.
[43] 李京,王悦,宋玉娟,等. 首批低分子肝素相对分子质量国家对照品的建立[J]. 中国药学杂志,2020,55(10):824-837.
[44] MCCART G M,KAYSER S R. Therapeutic equivalency of low-molecular-weight heparins[J]. Ann Pharmacother,2002,36(6):1042-1057.
[45] MAI V,TANGUAY V F,GUAY C A,et al. DOAC compared to LMWH in the treatment of cancer related-venous thromboembolism:a systematic review and meta-analysis[J]. J Thromb Thrombolysis,2020,50(3):661-667.
(收稿日期:2020-11-17 修回日期:2021-03-15)
(編辑:胡晓霖)
猜你喜欢 系统评价癌症 治癌症,生存质量很重要家庭科学·新健康(2019年1期)2019-03-06放疗小雪花·初中高分作文(2018年4期)2018-12-12瓜蒌薤白半夏汤治疗不稳定型心绞痛的Meta分析中国民族民间医药·上半月(2018年5期)2018-09-18活血化瘀药治疗椎动脉型颈椎病的Meta分析风湿病与关节炎(2017年11期)2017-12-06中国癌症分布图瞭望东方周刊(2017年36期)2017-09-28认知训练改善卒中后认知功能障碍的系统评价中国民族民间医药·下半月(2017年4期)2017-05-12癌症是怎么形成发展的家庭科学·新健康(2016年6期)2016-06-30主动出击:将癌症消灭在萌芽状态大众医学(2016年4期)2016-05-26大学生主观幸福感干预措施综述新校园·上旬刊(2016年2期)2016-04-27沙美特罗替卡松与噻托溴铵联合吸入对稳定期中重度慢性阻塞性肺疾病患者疗效的系统评价中国医药导报(2015年24期)2015-09-11




